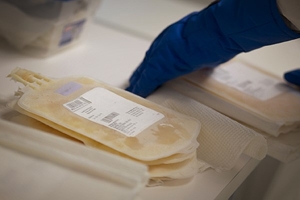
隨著細胞與基因治療的快速發展,產品的安全性、一致性、量產可行性及監管符合性是商業化成功的核心挑戰。無血清培養基(Serum-Free Medium, SFM)在細胞治療產品的製程開發中扮演著愈發關鍵的角色。傳統上,胎牛血清(Fetal Bovine Serum, FBS)廣泛用於細胞培養,但血清的批次差異及潛在病原體風險,促使無血清培養基成為製程開發的關鍵解決方案及主流選擇。本文將深入分析無血清培養基的技術趨勢、應用優勢,以及如何推動細胞治療產業的標準化與規模化。
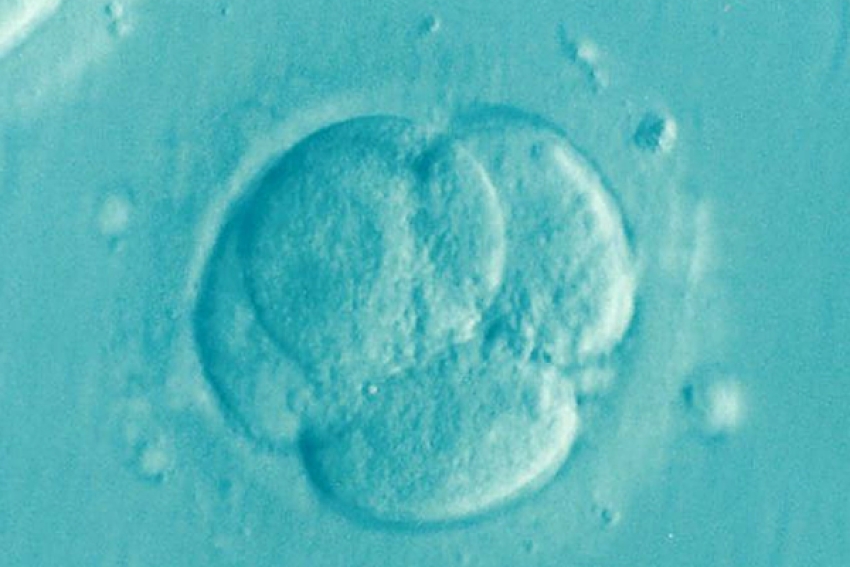
人類血小板(human Platelet Lysate, hPL)用於幹細胞治療之應用
十一月 12, 20182005年研究發現使用人類血小板裂解濃縮液(human Platelet Lysate, hPL)可以用來培養hMSC,對人體細胞治療臨床應用來說,HPL提供了一個新的選擇,利用HPL可以建立一個Xeno-free的細胞培養環境,在以細胞治療為目的細胞培養應用上相對更安全。
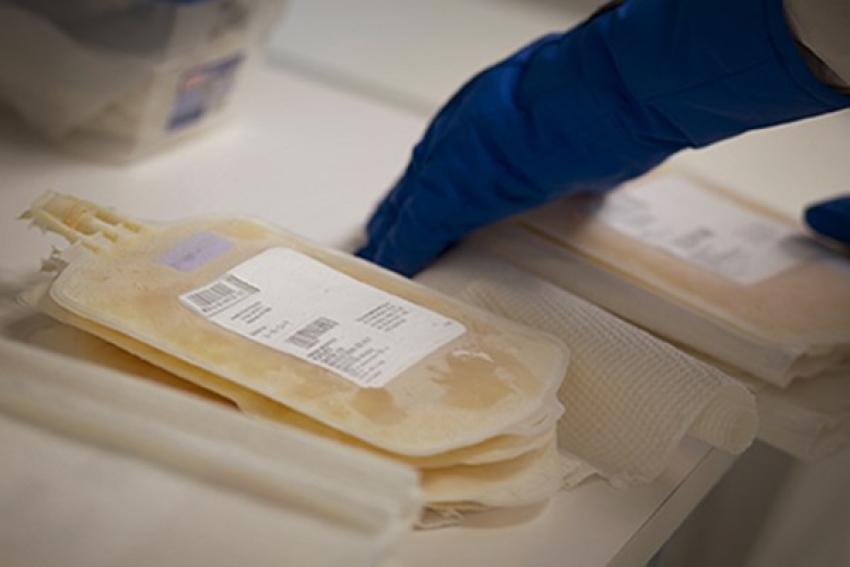
T Cell 體外放大培養-無血清培養基之選擇及應用
九月 16, 2018大部分的免疫細胞治療在生產過程中,都必須經過體外細胞擴增的步驟,這也是很重要且關鍵的一個部分,細胞必須能夠穩定、有效且安全的方式在體外環境擴增,其中很重要的輔助性材料之一就是培養基。
Thermo Fisher 宣布收購BD的先進生物加工業務,拓展生物製程
九月 15, 2018馬薩諸塞州沃爾瑟姆,2018年9月7日 /新華美通/ -賽默飛世爾科技公司(紐約證交所代碼:TMO),科學服務領域的世界領導者,已與BD(碧迪公司的最終協議- NYSE:BDX ),一家全球領先的醫療技術公司,Thermo Fisher將收購BD的先進生物加工業務。
輔助性材料(Ancillary materials)之品質管理
八月 23, 2018輔助性材料的品質管理對於細胞治療產品也是很重要的一環,這將會影響細胞產品最後的安全性及有效性等問題,若沒有做好品質控管則可能會導致產品暴露在高風險的狀態,發生巨額的損失。
New Articles
Cell Therapy











![衛福部核可之細胞治療執行單位 [持續更新]](https://biomaptw.com/media/k2/items/cache/753a82091bdf93df272697e1f26229c2_XL.jpg)