本文針對2023年Frost & Sullivan評選未來2-4年內將對社會產生重大影響之3項健康照護新興技術,分別為:無細胞生物製造技術、微型工程器官、抗衰老療法等,介紹其定義、應用範疇、技術特點、代表性案例與發展趨勢等。
一、前言
Frost & Sullivan在評估市場潛力、專利申請活動、募資狀態、2023年主流趨勢、經濟影響等關鍵要素後,於健康照護領域中,選出多項未來2-4年內將對社會產生重大影響的新興技術,包括:無細胞生物製造技術 (Cell-free biomanufacturing)、微型工程器官(Micro-engineered organs)、抗衰老療法 (Senotherapeutics)、胞泌體療法(Exosomal therapies)、精準分子檢測 (Precision molecular testing)、空間體學(Spatial omics)等。本文針對前3項新興技術,分述其定義、應用範疇、技術特點、代表性案例等(各項新興技術摘要與發展潛力請參閱圖一)。
二、無細胞生物製造技術(Cell-free biomanufacturing)
無細胞生物製造技術為不需要利用細胞生產生物分子的技術。該技術萃取出細胞內參與轉錄與轉譯必須的酵素、DNA模板、胺基酸等分子,於體外受控環境下執行一系列的生物化學反應來合成需要的生物分子產品(如疫苗、酵素)。
(一) 技術特性與優勢
無細胞生物製造技術可以用來生產複雜蛋白質、疫苗、小分子藥物、診斷試劑、食品添加物、化學藥品等產品。與利用細胞生產相比,其技術特點及優勢包含:
(1) 快速並可依需求生產:具備簡易(不須培養細胞)以及能快速生產之優勢,並且能依照需求生產合適且適量的生物分子,可於照護點(Point-of-Care, POC)生產疫苗與個人化藥物,或可於戰場或太空任務等資源有限的環境中生產。
(2) 高靈活性且可即時優化生產流程:能即時監控生物分子產品生產製造的各個步驟與流程,並能即時進行修改與調整參數。相較於傳統利用微生物或細胞生產產品,無細胞生物製造不須將細胞生長條件等因素納入考量,能更輕易地實現製程優化。
(3) 更低的碳足跡和基礎設施成本:由於無細胞生物製造不需要大型的基礎設備(如大型發酵槽),因此該技術的基礎設施成本較低,且具備更少的碳足跡。
(二) 代表性案例
(1) 以植物之蛋白質生產路徑為基礎的無細胞生產系統-ALiCE
開發廠商:德國LenioBio
德國的LenioBio利用菸草細胞之粒線體以及生產蛋白質所需之酵素與生物分子,開發出無細胞生產系統ALiCE,能在48小時內生產高濃度(3克/公升)複雜結構的蛋白質,包括抗體、膜蛋白、類病毒顆粒(Virus-like particle, VLP)等。該平台具備生產靈活、可擴充等特性,生產規模可從個人化醫療的單劑量到疫苗大規模生產(50000劑量)。
(2) 治療性蛋白質藥物與疫苗的無細胞蛋白質製造平台-XpressCF
開發廠商:美國Sutro Biopharma
Sutro Biopharma開發的無細胞蛋白質製造平台XpressCF,能在DNA合成後的數天內客製化生產治療性蛋白質和疫苗,並且可迅速放大生產規模。此外,Sutro Biopharma也開發出新一代的蛋白質製造平台XpressCF +,能於蛋白質中插入非天然(non-natural)氨基酸,以調整蛋白質的特性,如提升與小分子藥物的結合能力形成更穩定的抗體藥物複合體(Antibody-drug conjugates, ADC),進而提升藥物療效。Sutro Biopharma近期積極與BioNova、Vaxcyte等藥廠合作開發ADC候選藥物或疫苗。
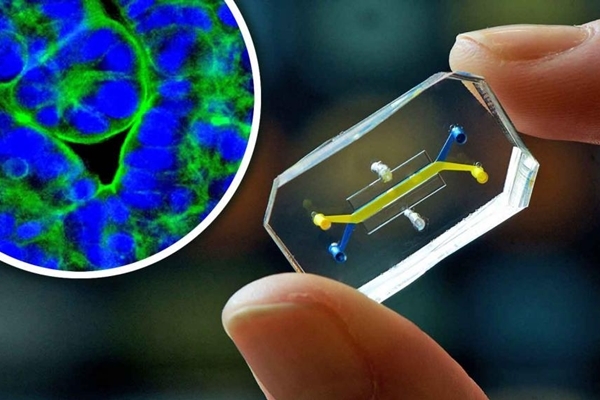
三、微型工程器官(Micro-engineered organs)
微型工程器官旨,包括器官晶片(organs-on-chips, OOC)和類器官(organoids)。類器官為根據發育生物學,提供幹細胞合適的生長環境(如特定的生長因子),使其自行分化與組織形成的三維細胞複合體。器官芯片則是將細胞(通常為已分化之幹細胞)培養於特殊設計的微流道晶片上。微型工程器官能模擬天然器官與系統之結構與功能,可應用於疾病模擬、藥物發現、藥物毒性測試和組織工程等。
(一) 技術特性與優勢
目前用於臨床試驗的動物模型,往往會因不同的實驗物種選擇,而產生極大的差異,同時試驗動物也難以精準地模擬人體器官的功能與生化反應。另外,使用試驗動物亦有嚴重的道德疑慮。微型工程器官能更精準地模擬人體器官,甚至於可同時模擬多個器官,有助於了解器官之間的交互作用以及疾病進程。其他優勢包括:減少臨床前以及臨床試驗的時間、減少藥物開發的花費、減少試驗動物的數量、可以作為個人化醫療(如個人化藥物篩選)、即時觀察藥物反應結果。
(二) 代表性案例
(1) 大腸與小腸類器官- RepliGut
開發廠商:美國Altis Biosystems
美國的Altis Biosystems推出能模擬大腸與小腸的類器官平台-RepliGut。RepliGut能讓幹細胞分化成上皮細胞,並且整齊排列於設計的支架結構上,形成單層上皮組織,以模擬大腸與小腸的表皮結構。該平台可以應用於藥物篩選、疾病影響研究、腸道微生物研究。
(2) 腦、十二指腸、肝晶片等多款器官晶片
開發廠商:美國Emulate
Emulate開發出多款器官晶片,包括腦晶片(Brain-Chip)、十二指腸晶片(Duodenum Intestine-Chip)、肝晶片(Liver-Chip)等。其中,腦晶片能培養腦部的多種細胞,包括神經元(neurons)、星形膠質細胞(astrocytes)、腦微血管內皮樣細胞(brain microvascular endothelial-like cells),能模擬腦部複雜的神經與血管結構以及血腦屏障;十二指腸晶片結合了十二指腸類器官和小腸微血管內皮細胞,並能模擬腸道的蠕動環境,可望應用於十二指腸生理學、藥物吸收和腸道藥物相互作用等研究;肝晶片則能模擬肝細胞之生長環境,包括組織之3D結構與血液流動等,能應用於藥物毒性研究以及腺相關病毒(adeno-associated virus, AAV)基因療法的安全性評估。
四、抗衰老療法(Senotherapeutics)
多數國家人口面臨高齡化問題,因此,抗衰老療法的發展備受重視。抗衰老療法包括使用如小分子、細胞療法、基因編輯等藥物,清除衰老細胞,或是調節生理機能來停止或逆轉衰老進程,以改善個人的健康從而延長壽命。
(一) 療法類型與研究動向
常見的抗衰老療法涵蓋:抗衰老藥(senolytics),能抑制與調節衰老細胞的抗凋亡路徑(Snc antiapoptotic pathways, SCAP),誘使衰老細胞凋亡,為目前最被廣泛研究抗衰老療法;衰老阻斷劑(senoblockers),目標為逆轉細胞的衰老以及再生衰老的組織;衰老抑制劑(senosuppressors),可抑制衰老細胞的產生;衰老調節劑(senomodulators),主要功能為調節SASP(senescence-associated secretory phenotype)的分泌或干擾其生成。SASP為衰老細胞分泌的酵素、生長因子等生物分子的統稱,這些生物分子會促使周邊細胞發炎,並導致代謝異常、免疫失調、神經疾病等多種疾病。
目前的研究動向為利用體學分析、人工智慧技術等技術尋找新的藥物標靶並確認新藥物與衰老之關聯性,以及了解抗衰老療法對人體的長期影響。另外,利用機能性食品或保健食品延緩衰老,如類黃酮、益生菌,亦是抗衰老療法關注的焦點。
(二) 代表性案例
(1) 誘使衰老細胞凋亡之DNA藥物與遞送載體-SENSOlytic平台
開發廠商:美國Oisin Biotechnologies
美國Oisin Biotechnologies開發了SENSOlytic平台。該平台使用蛋白脂質載體(proteo lipid vehicle, PLV)裝載DNA藥物。當PLV注入體內後,會進入到每一個接觸到的細胞。該藥物僅會誘發衰老細胞或癌細胞凋亡,對健康細胞無害。前述療法已在多種試驗動物中被證明可以有效地消除全身的衰老細胞,並且能延長小鼠的壽命。
(2) AI衰老藥物發現平台-Alembic藥物發現平台
開發廠商:美國Rubedo Life Science
美國Rubedo Life Sciences推出以人工智慧為基礎的Alembic藥物發現平台以及藥物化學技術SenTech。Alembic能分析單細胞RNA定序(scRNAseq)與體學數據,識別出衰老疾病特有之特徵資訊,並且找出最合適的藥物靶標。SenTech則可設計出比現有藥物具有更安全性與選擇性的小分子藥物。目前Rubedo Life Sciences著重於衰老相關之慢性皮膚炎、肺纖維化、肌少症等疾病的藥物開發。










![衛福部核可之細胞治療執行單位 [持續更新]](https://biomaptw.com/media/k2/items/cache/753a82091bdf93df272697e1f26229c2_XL.jpg)