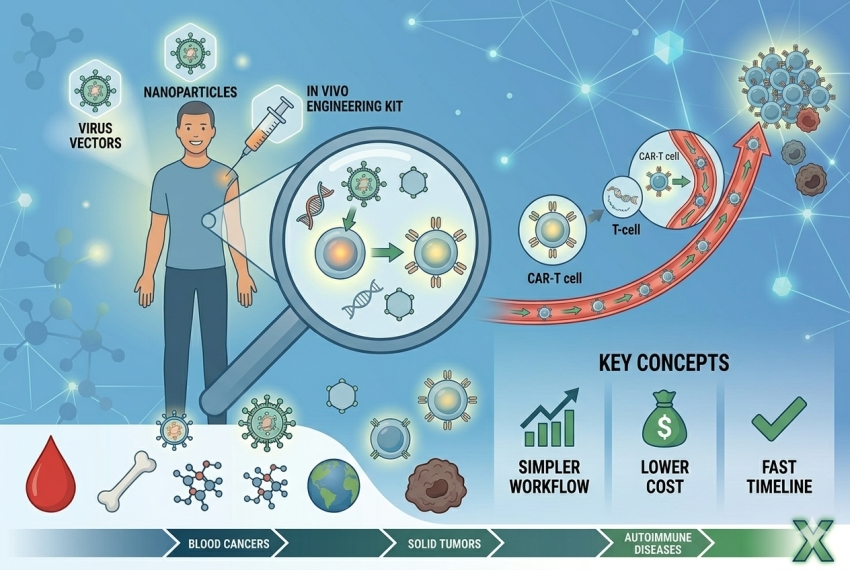
嵌合抗原受體 (Chimeric antigen receptor, CAR) T細胞療法被視為某些血液惡性腫瘤的突破性治療方法,在T細胞上工程化表現CAR使其能夠標靶針對血癌細胞。第一代CAR包含細胞外抗原結合區域連接細胞內訊號傳遞區域如T細胞受體的CD3ζ鏈。第二代CAR利用融合至CD3ζ鏈的共刺激結構區域,例如CD28或CD137 (也稱4-1BB)來增強CAR-T細胞活性和持續性。患者自體的第二代CAR-T細胞療法已經被核准了三種藥物,依據核准時間分別是Kymriah (tisagenlecleucel, Novartis藥廠)治療復發型或難治型B細胞急性淋巴細胞白血病、Yescarta (axicabtagene ciloleucel, Kite/Gilead藥廠)治療復發型或難治型瀰漫性大B細胞淋巴瘤及Tecartus (brexucabtagene autoleucel, Kite/Gilead藥廠)治療復發型或難治型被套細胞淋巴瘤 (表1)。
|
藥品名 |
藥廠 |
核准時間 |
核准適應症 |
藥價 (劑/萬元) |
|---|---|---|---|---|
|
Kymriah |
Novartis |
2017.08 |
復發或難治型B細胞急性淋巴細胞白血病 |
47.5 |
|
2018.05 |
復發或難治型大B細胞淋巴瘤 |
|||
|
Yescarta |
Kite/Gilead |
2017.10 |
復發或難治型大B細胞淋巴瘤 |
37.3 |
|
Tecartus |
Kite/Gilead |
2020.07 |
被套細胞淋巴瘤 |
37.3 |
資料來源:工研院產科國際所 ITIS研究團隊 (2021/1)
雖然CAR-T細胞療法十分有潛力用於血液腫瘤治療,但自體CAR-T細胞療法需要為每個病患量身訂製,製造與治療間的物流增加了醫病間的不確定性與複雜性。且自體CAR-T迄今仍有許多缺點待改善,例如製造成本高昂、某些病患的T細胞容易製造失敗以及目前製造過程約需3週,這些缺陷加深了病患可獲得治療的時間壓力。尤其在某些高度急性白血病的患者中,在製造自體CAR-T細胞時腫瘤可能已加速進展,或者由於先前一、二線治療相關的原因而無法使用自身T細胞。由於腫瘤微環境的多種免疫抑制機制造成T細胞功能障礙,病患自體T細胞也可能導致治療無效。不僅如此,這種複雜的治療本身製造成本仍然很高,對醫療保健系統構成沉重的挑戰。
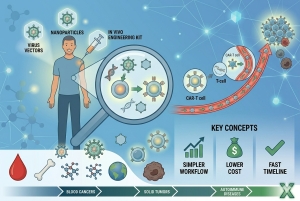
使用來自健康捐贈者的細胞,也就是製造現貨型(off-the-shelf)同種異體(allogeneic) CAR-T細胞有潛力解決上述問題。同種異體CAR-T細胞具有能夠規模化製造來降低成本,單一捐贈者可以生產大量CAR-T細胞(圖1)。
此外,製造同種異體CAR-T細胞能夠產生數百劑量冷凍保存的T細胞,使患者可以隨時取用立即進行治療或重新再給藥,不會因製造或生產規模而造成延誤治療。現貨型簡化了捐贈細胞的選擇性和製造CAR-T細胞的標準化過程,不像是自體CAR-T細胞是製造患者產品的唯一機會,而同種異體細胞的生產則能夠產生一批細胞產品。不僅如此,現貨型同種異體CAR-T細胞也可能設計成同時針對不同標靶的細胞產品組合(表2)。
不過,源自健康同種異體捐贈者的細胞療法仍有一些議題待解決,一是細胞來源,二是同種異體T細胞的組織相容性可能會導致危及病患生命的移植物抗宿主疾病(GvHD),且可能會被病患宿主的免疫系統迅速清除,限制抗腫瘤活性。
|
特徵 |
自體CAR-T細胞 |
同種異體CAR-T細胞 |
|---|---|---|
|
捐贈者來源 |
病患本身 |
健康捐贈者 |
|
生產製造過程 |
牽涉複雜的物流;從白血球分離術到CAR-T細胞輸液的時間差;患者的免疫狀態和先前接受的治療造成T細胞差異性 |
可以規模放大的製造流程,即從單一捐贈者生產並冷凍保存大量CAR-T細胞;即用於患者治療的藥物批次控管;T細胞特性接近標準化 |
|
臨床適應症 |
血液惡性腫瘤(已核准);實體腫瘤(臨床試驗中) |
血液惡性腫瘤;實體腫瘤 (皆臨床試驗中) |
|
主要議題/風險 |
細胞激素釋放症候群*;CAR相關基因修飾;CAR-T會造成B細胞再生障礙 |
細胞激素釋放症候群*;CAR和/或基因編輯相關的基因修飾;移植物抗宿主疾病**;嚴重淋巴細胞清除造成的毒性 |
|
持續性 |
中長期(數月到數年) |
短中期(數周到數月) |
|
多次劑量 |
受限於病人細胞數 |
不受細胞數量的限制,但具有同種免疫的風險 |
|
成本 |
目前極高(將來可能會減少) |
預期為中等 |
註:*細胞激素釋放症候群: Cytokine release syndrome; **移植物抗宿主疾病: graft versus host disease (GvHD)
資料來源:工研院產科國際所 ITIS研究團隊 (2021/1)
(一)細胞來源
1. 利用幹細胞衍生現貨型CAR-T
目前用於製造CAR-T的T細胞主要來源是周邊血單核球細胞(peripheral blood mononuclear cell, PBMC),較少來自臍帶血 (umbilical cord blood, UCB)。這些T細胞也可以衍生自能夠自我再生的幹細胞,例如誘導性多能幹細胞(induced pluripotent stem cells, iPSC)或胚胎幹細胞。因為來自不同健康捐贈者的周邊血,有機會建立不同亞型之人類白血球抗原(HLA)複合體的細胞庫,以選擇與患者的HLA類型配對的細胞批次。且與患者自體T細胞相比,同種異體CAR-T細胞是由健康細胞產生的,其較不受癌症免疫抑制作用或接受化療的影響。
臍帶血衍生的CAR-T細胞可降低GvHD的發生率和嚴重性,減少對HLA差異的嚴格限制,因為源自臍帶血的T細胞具有較低的同種異體反應性。此外,臍帶血T細胞還具有降低活化T細胞核因子(nuclear factor of activated T cells, NFAT)訊號傳導以減少異原性反應,減少GvHD的風險。另外利用胎盤來源的幹細胞可用於產生T細胞或自然殺手細胞,因為胎盤幹細胞僅表現少數HLA型態,甚至不表現HLA,大大降低移植排斥的風險。
來自誘導性多能幹細胞的T細胞來源,理論上擁有無限的自我更新能力,並且可以存入細胞庫無限期使用。使用誘導性多能幹細胞的一個優勢是CAR-T細胞是從同一個克隆改造的多能細胞產生的,因此是同質的。再利用基因編輯消除誘導性多能幹細胞上的HLA分子以避免排斥。但誘導性多能幹細胞的致癌性仍有很大疑慮。
目前有幾種策略去除或減少T細胞受體(T cell receptor, TCR)複合體的表現。一種方法是在T細胞中表現截短的CD3ζ 區域當作TCR抑制分子,降低TCR訊號傳遞以防止異體移植的排斥。或利用shRNA來降低TCR的表現,但上述方法仍可能保留少量但具功能的TCR,因此目前多數技術開發選擇使用基因編輯來確保完全去除TCR。TCR蛋白複合體由α鏈和β鏈(αβΤ細胞)組成,編碼β鏈基因含兩個恆定區,編碼α鏈的基因只有一個恆定區,因此破壞T細胞受體α鏈恆定區(TRAC)的基因是破壞αβTCR的最直接方法,使細胞無法形成TCR複合體。
αβT細胞目前是CAR-T細胞來源的黃金標準,但αβT細胞不是唯一的選擇。存在於周邊血中的NK細胞可以離體擴增並工程化細胞,裝載CD19修飾的CAR-NK細胞初步在臨床試驗中已顯示抗血液腫瘤活性。NK T細胞是表現NK細胞表面標誌的淋巴T細胞的一種,恆定NK T細胞(invariant NKT, iNKT)幾乎不表現TCR不僅降低移植物抗宿主的風險,且利用CD19及CD1d修飾的CAR-iNKT具有很強的抗淋巴瘤特性。
γδT細胞是預期不會引起移植物抗宿主的效應細胞,僅佔循環淋巴細胞的1-5%,主要存在於一些上皮細胞。γδT細胞具有易於利用天然配體刺激擴增及穿透實體腫瘤的潛在優勢。
降低同種異體T細胞療法中移植物抗宿主風險的另一種潛在方法是使用健康人體的具病毒特異性T (virus‐specific T, VST)細胞,純化記憶性病毒特異性T細胞讓針對病毒疾病的治療更有專一性,且在臨床實驗中也觀察到甚少的移植物抗宿主疾病徵兆。因此,一些生物科技公司正在開發基於同種異體第四型人類皰疹(Epstein-Barr, EB)病毒特異性T細胞的CAR-T療法。裝載CD19的EBV特異性CAR-T細胞透過內源性病毒特異性TCR識別並殺死淋巴瘤細胞。類似的策略也已擴展到實體腫瘤標靶,裝載標靶雙唾液酸神經節苷脂 (disialoganglioside, GD2)的自體EBV特異性CAR-T細胞用來治療神經母細胞瘤。但此技術的移植物抗宿主疾病及抗腫瘤活性仍需臨床證明。
雖然CAR-T細胞療法已經改變了某些血液惡性腫瘤的治療模式,也可能是癌症治療中最具前景的方法之一,開發病患易獲得的治療方式及降低製造成本的現貨型CAR-T將顯著增加治療的可及性。基因編輯技術已經透過有效消除TCR表現來控制移植物抗宿主疾病的風險,並且也已經利用基因編輯開發出使同種異體CAR-T細胞躲過宿主免疫系統的新技術。雖然基因編輯可以在同種異體CAR-T細胞中結合多種基因修飾,但多重基因修飾後脫靶基因可能導致的致癌風險,仍需滿足嚴格的品質控制和法規認證程序。在提高CAR-T細胞的功效方面,尤其是在實體腫瘤治療仍有許多挑戰尚待突破,也就是在免疫抑制的情況下具有更適合的腫瘤選擇性、更好的腫瘤進入能力和更高的抗癌活性。為了改善自體CAR-T細胞製造的時間成本、無法隨時治療、被自身腫瘤污染的細胞來源、T細胞突變、T細胞擴增不足及T細胞功能障礙的未滿足需求,使用基因編輯的現貨型CAR-T細胞已經開始進入臨床試驗,做為免疫腫瘤學在血液惡性腫瘤治療和實體腫瘤治療的臨床突破。
參考資料:
1. Nature Reviews Drug Discovery, Volume 19, pages185–199, 2020
2. Advances in Cell and Gene Therapy, Volume3, Issue3, July 2020
資料來源: 經濟部技術處










![衛福部核可之細胞治療執行單位 [持續更新]](https://biomaptw.com/media/k2/items/cache/753a82091bdf93df272697e1f26229c2_XL.jpg)