長期以來,細胞免疫療法在血液型癌症(如白血病)中取得顯著成功,但對於佔全球癌症死亡大宗的「實體腫瘤」,始終面臨療效有限的挑戰。然而,最新由National Cancer Institute(NCI)發布的研究顯示,一種結合個人化免疫細胞與免疫檢查點抑制劑的策略,正為實體腫瘤治療帶來重要轉機。
再生醫療可以治療癌症嗎?你該知道的關鍵風險
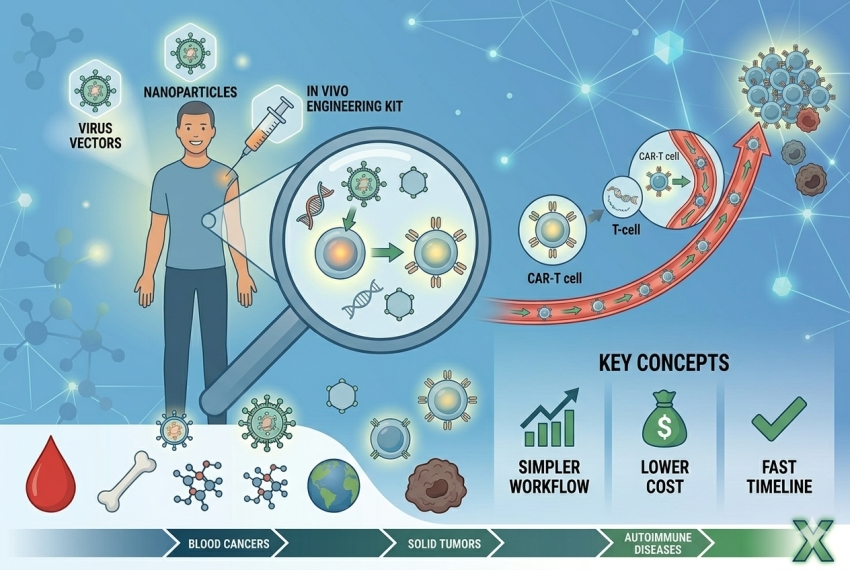
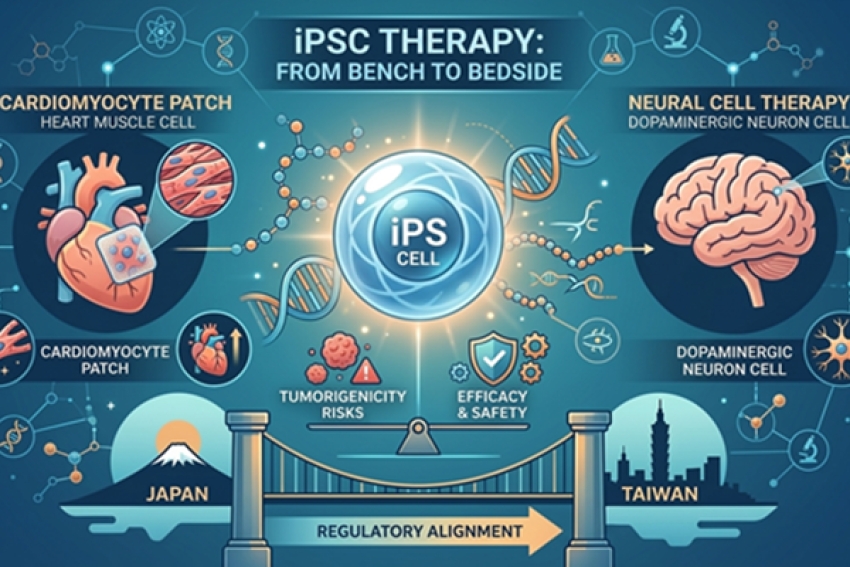
十二月 26, 2025隨著醫學與科技的創新發展,「再生醫療」逐漸成為一個新興話題。「再生醫療」主要利用人體細胞的再生能力,修補受損組織與器官,這種從傳統破壞性清除式療法已經轉變為修復導向與免疫調節。再生醫療結合了細胞治療、基因治療、組織工程及外泌體等多方技術,為過往傳統醫療難以治癒的疾病帶來新的希望,其中大宗為癌症治療。
突破「去勢抵抗」的困境:前列腺癌治療的新希望
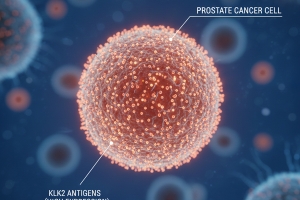
十二月 13, 2025前列腺癌是全球男性第二常見的癌症,早期診斷與治療效果良好。然而,一旦疾病進展至轉移性去勢抵抗性前列腺癌(mCRPC)階段,治療選項便會大幅受限,成為醫療上的一大瓶頸。近日,醫藥巨頭強生公司(Johnson & Johnson)旗下的雙特異性抗體新藥 JNJ-78278343 (Pasritamig) 注射液,被中國藥監機構列入「擬納入突破性治療品種」名單,標誌著前列腺癌的治療可能迎來一個關鍵的轉折點。這項創新療法如何應對當前的治療困境?
FDA批准第一個TIL療法用於治療晚期黑色素瘤
四月 22, 2024經過三十多年的醞釀,美國食品藥物管理局 (FDA) 批准了 lifileucel (Amtagvi),這是第一個使用稱為腫瘤浸潤淋巴細胞 (TIL) 的免疫細胞治療癌症的方法。該機構於 2024年 2 月 16 日宣布的決定也使 lifileucel 成為第一個被批准用於治療實體腫瘤(皮膚癌黑色素瘤)的細胞療法。與CAR T 細胞療法(另一種細胞療法)的情況一樣,lifileucel 是使用患者自身的T 細胞製成的。對於這兩種療法,細胞都是在患者接受治療的醫院收集的,但會被送到最終的治療中。
免疫療法藥物組合成為晚期肝癌治療趨勢
二月 05, 2023根據世界衛生組織的最新統計,2020年肝細胞癌是全球第六大癌症,發生人數達90.6萬人,也是癌症死亡的第三位原因,約83.0萬病例,占所有癌症死亡的8.3%。
New Articles
Cell Therapy











![衛福部核可之細胞治療執行單位 [持續更新]](https://biomaptw.com/media/k2/items/cache/753a82091bdf93df272697e1f26229c2_XL.jpg)