胰臟癌存活率低,是攸關全人類健康的重大議題。李文華院士帶領的研究團隊曾於2015年發現,胰臟癌腫瘤細胞的細胞膜上會出現大量受體 「IL-17RB」,與配體相互結合後,便會啟動一連串反應,刺激細胞增生或轉移。團隊據此研發抗體藥物,藉由減少IL-17RB與配體「IL17B」結合機會,降低癌細胞轉移機率。鑽研胰臟癌多年、同時也是團隊成員的中研院基因體中心胡春美助研究員表示,當時已確認受體IL-17RB是刺激胰臟癌細胞轉移的重要因素,但仍不清楚分子內部的訊息傳遞機制。團隊參考肺癌「表皮生長因子受體(EGFR)」 抑制劑的研發歷程後,認為此項胰臟癌研究值得持續推進,以進一步改善胰臟癌治療效果。
後續研究發現,IL-17RB不僅出現在癌細胞上,也會出現在正常免疫輔助型T細胞(Th2)上,而且免疫細胞若缺乏IL-17RB,反而影響免疫訊息傳遞,導致人體容易受微生物感染。因此,最佳治療方法是了解IL-17RB於癌細胞與免疫細胞上的差異,再發展標靶藥物。如此一來,可在不影響患者免疫能力的前提下,同時防範癌細胞擴散。
經過多年反覆驗證,研究團隊終於成功破解IL-17RB的致癌機制,並合成出一種多胜肽分子,可有效解決上述難題。論文第一作者、中醫大吳恒祥助理教授解釋,不同於免疫細胞,在胰臟癌細胞表面大量出現的IL-17RB,容易兩兩結合,形成同質雙聚體。當同質雙聚體遇到配體IL-17B後,就會召喚激酶「MLK4」,催化蛋白質磷酸化,有如按下開關般,啟動後續一連串致癌訊號。研究團隊設計出的多胜肽分子是一組胺基酸序列,可在細胞內特定位置取代激酶MLK4,與受體IL-17RB結合,阻止激酶與受體交互作用,藉此阻斷癌化訊號傳遞。
研究團隊表示,此多胜肽分子可以在胰臟癌細胞內找到正確「鑰匙孔」並事先「卡位」,防止激酶MLK4前來「解鎖」啟動反應開關;相較於先前研發的抗體藥物,治療更為精準,不影響患者免疫力。實驗結果顯示,罹患胰臟癌的小鼠若施打此種胜肽分子,癌細胞轉移至肝臟與肺臟的機率大幅下降,壽命也因此延長。未來團隊期望能繼續深化研究,研發出效果更穩定的小分子藥物,協助胰臟癌患者進行標靶治療。
本研究論文為 ”Characterization of Initial Key Steps of IL-17 Receptor B Oncogenic Signaling for Targeted Therapy of Pancreatic Cancer”。研究團隊成員有中研院李文華院士、胡春美助研究員和沈家寧副研究員;中國醫藥大學吳恒祥助理教授;臺大醫院田郁文醫師、張毓廷醫師、章明珠醫師和鄭永銘醫師。
論文全文:https://stm.sciencemag.org/content/13/583/eabc2823
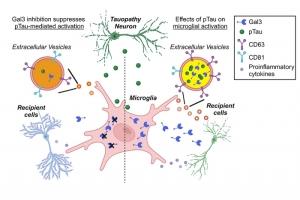
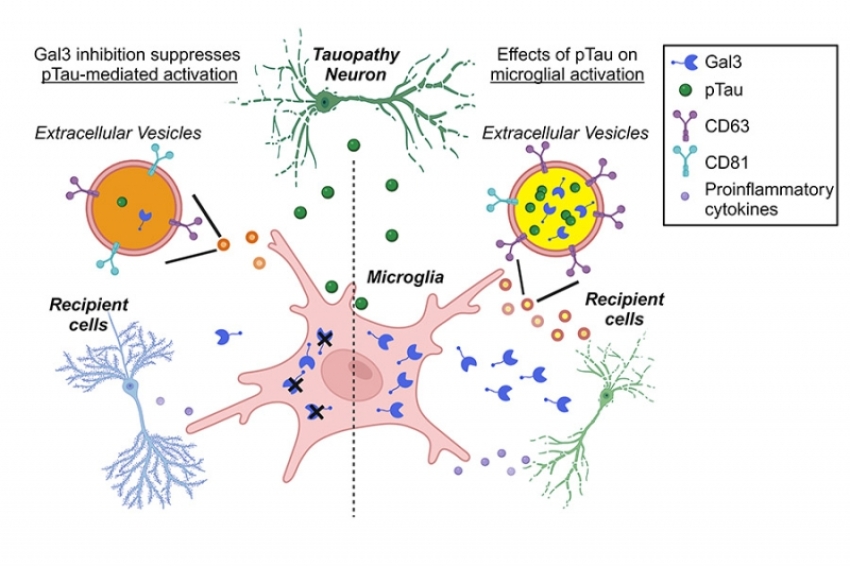
說明:此圖左半邊為正常免疫輔助型T細胞 (Th2),受體IL-17RB在此可以傳遞免疫反應訊號。此圖右半邊為胰臟癌細胞,IL-17RB在癌細胞上反而會召喚激酶MLK4,啟動致癌反應。研究團隊合成的多胜肽分子,可與激酶MLK4競爭,阻止激酶與受體IL-17RB結合,藉此阻斷後續癌化訊息傳遞。

說明:在癌細胞膜表面,受體IL-17RB大量出現,因此配體IL-17B結合後會形成同質雙聚體,同質雙聚體找到後,就會在細胞內部召喚激酶MLK4,啟動致癌訊號,催化癌細胞增生及移轉。










![衛福部核可之細胞治療執行單位 [持續更新]](https://biomaptw.com/media/k2/items/cache/753a82091bdf93df272697e1f26229c2_XL.jpg)