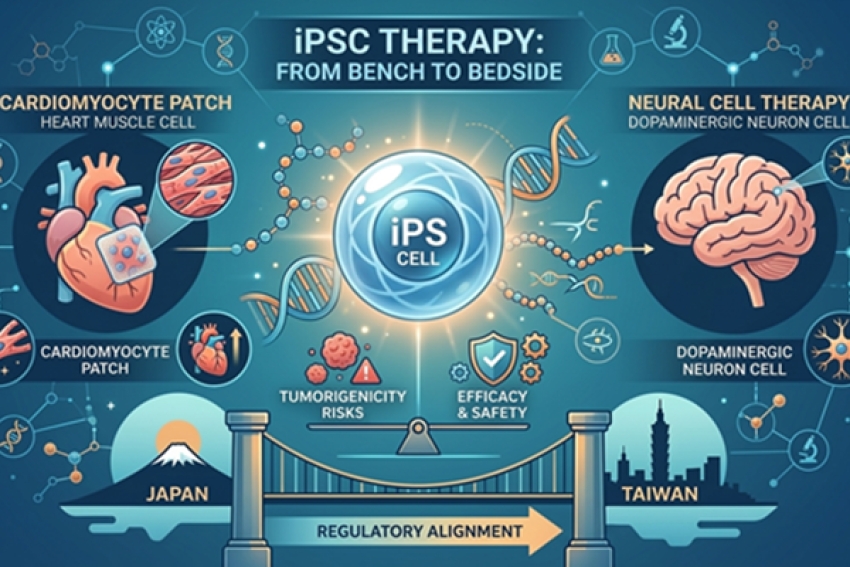
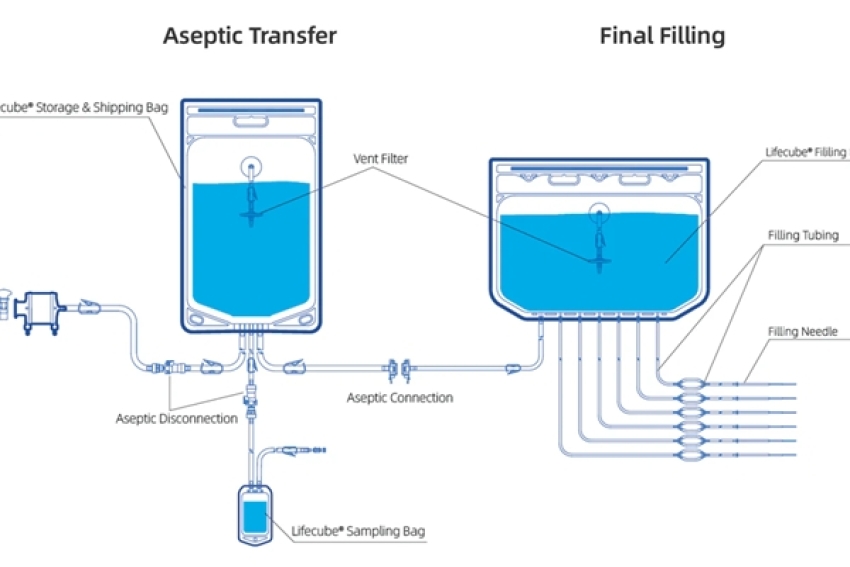
在iPS技術尚未發明前,科學家研究幹細胞必須取自類胚胎或研究動物的胚胎,在道德上總是引起不少爭議,而iPS的發明讓科學家取得多功能幹細胞有了新的方法,透過基因重編輯技術,可將已分化的特定成體細胞再回到較原始的未分化狀態,iPSC也經過驗證,該細胞和人類胚胎幹細胞(ESC)一樣,都能保有多功能分化的特性。現在科學家只要在實驗室就能輕鬆產出iPSC,先不論iPSC未來是否能真的應用的臨床,但已提供科學家方便的幹細胞來源來進行研究。
誘導性多能幹細胞(Induced pluripotent stem cell, iPSC),又稱人工誘導多能幹細胞,透過病毒載體將特定外源性的轉錄因子基因包括Oct4、Sox2、c-Myc、Klf4轉殖入哺乳動物成體細胞,並誘導該基因的表現,進而將該成體細胞的基因做重新編成,形成的多能幹細胞,此過程又稱 reprogramming,該技術最早由日本科學家山中伸彌的研究團隊於2006年於小鼠細胞中發現,並在2007年確認該技術也可應用於人體細胞。
2012年科學家發表了CRISPR/Cas9的最新編輯技術,此技術可對細胞類染色體提供高專一性的編輯,此篇論文的作者則是想了解是否可透過利用CRISPR來調控內生性基因的表現讓細胞也發生reprogramming。實驗結果發現,不同於使用外源性基因的轉殖,透過CRISPR基因調控方式,只要單獨活化一個基因,Oct-4或Sox-2即可誘發細胞進行reprogramming,讓細胞回覆到具有多功能分化的原始特性。
Photo credit: National Institutes of Health (NIH) on Visualhunt.com / CC BY-NC










![衛福部核可之細胞治療執行單位 [持續更新]](https://biomaptw.com/media/k2/items/cache/753a82091bdf93df272697e1f26229c2_XL.jpg)